материал предоставил СИДОРОВ Александр Владимирович
Сплав — макроскопически однородная смесь двух или большего числа химических элементов. Сплавы получают путём:
- плавления — процесса перехода материалов из твёрдого состояния в жидкое при повышенных температурах;
- спекания — процесса получения твёрдых и пористых материалов из мелких порошкообразных или пылевидных материалов при повышенных температурах;
- осаждения из газовой фазы — процесса получение твёрдых материалов с помощью химических реакций, в которых участвуют газообразные реагенты.
Компоненты сплавов образуют между собой:
- твёрдые растворы — образуются в результате перехода в твёрдое состояния однородных жидких растворов, причём одно из веществ при этом сохраняет присущую ему кристаллическую решётку, а другое в виде отдельных атомов располагается в кристаллической решётке первого вещества, на основании чего различают твёрдые растворы:
- замещения, где часть атомов в кристаллической решётке одного вещества заменена атомами другого;
- внедрения, где атомы растворённого компонента внедряются в межатомарное пространство кристаллической решётки другого компонента (растворителя);
- химические соединения — сложные вещества, состоящие из химически связанных атомов двух или более элементов, причём возникающая при этом кристаллическая решётка упорядочена и отлична от кристаллических решёток элементов, образующих соединение;
- механические смеси — продукты смешения двух и более веществ, которые при кристаллизации не способны к взаимному растворению и не вступают в химическую реакцию с образованием соединения.
Кристаллизация — процесс выделения твёрдой фазы в виде кристаллов из растворов или расплавов.
Фаза — однородная часть термодинамической системы отделённая от других частей системы поверхностью раздела, при переходе через которую химический состав, структура и свойства вещества изменяются скачками.
Кристаллизация начинается при достижении некоторого предельного условия (переохлаждения жидкости, пересыщения пара), когда возникает множество мелких кристаллов — центров кристаллизации. Кристаллы растут, присоединяя атомы или молекулы из жидкости или пара (рисунок 1).
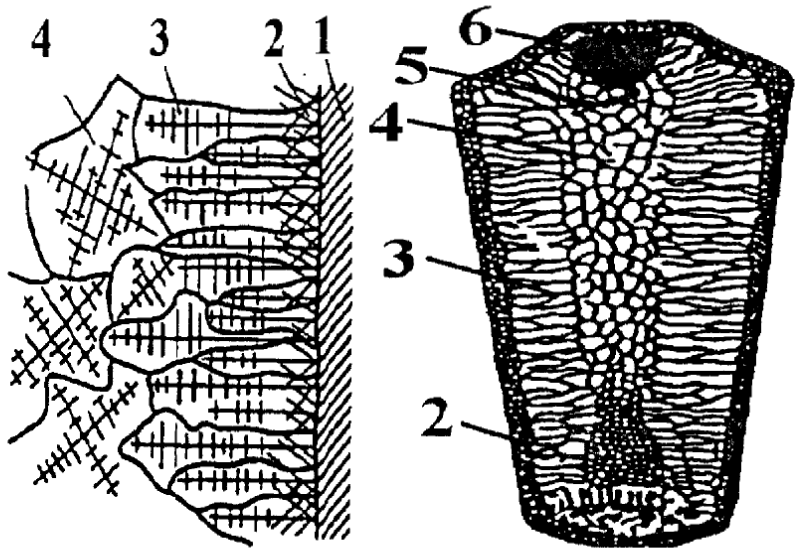
Рисунок 1 — Схема образования слитка спокойной стали в металлической изложнице: 1 — стенки изложницы; 2 — мелкие равновесные кристаллы; 3 — древовидные кристаллы; 4 — равновесные крупные неориентированные кристаллы; 5 — рыхлый усадочный слой; 6 — усадочная раковина
Критические точки — температуры, при которых изменяется строение материалов.
Кривые охлаждения — графическое изображение зависимости температуры от времени для материалов. Вид этих кривых свидетельствует о наличии или отсутствии фазовых превращений при некоторых определённых температурах или в интервале температур.
Диаграмма состояния — графическое отображение фазовых превращений материалов в зависимости от температуры. Для сплавов также в зависимости от концентрации входящих в них компонент.
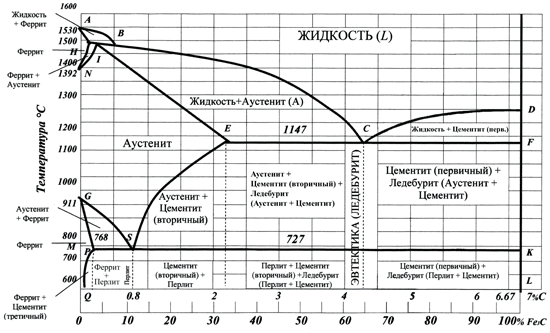
Так как на практике применяют металлические сплавы с содержанием углерода до 6,67%, то рассматривается часть диаграммы состояния от железа до цементита, содержащего углерод (рисунок 2).
Железо (Fe) — вязкий, пластичный металл серебристо-белого цвета, плотностью 7,87 т/м3, температурой плавления 1539 °С, быстро корродирует при высоких температурах или при высокой влажности на воздухе. В чистом кислороде железо горит, а в мелкодисперсном состоянии самовозгорается и на воздухе. Существуют следующие устойчивые модификации:
- от абсолютного нуля до 910 °C устойчива α-модификация с объёмноцентрированной кубической кристаллической решёткой (рисунок 3), после 910 °C теряет магнитные свойства (точка Кюри), переходя в δ-модификацию, которая отличается только размерами кристаллической решётки, поэтому отдельно не рассматривается;
- от 910 до 1400 °C устойчива γ-модификация с гранецентрированной кубической кристаллической решёткой;
- от 1400 до 1539 °C устойчива δ-модификация с объёмноцентрированной кубической кристаллической решёткой.
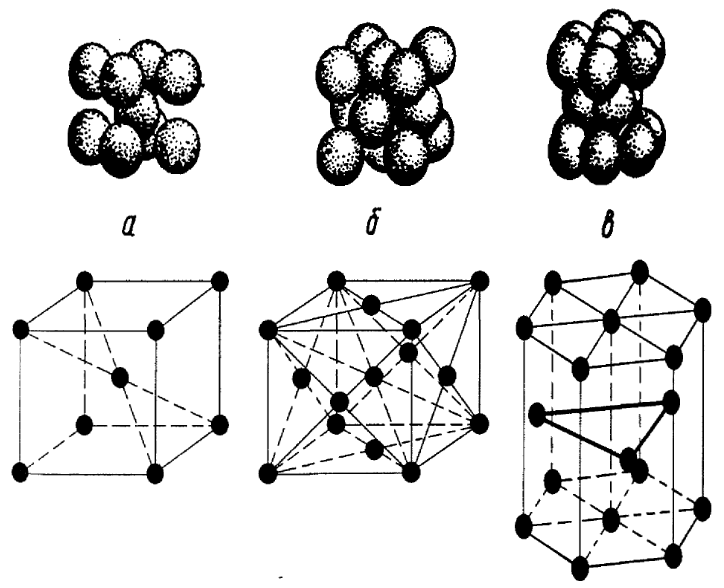
Рисунок 3 — Основные типы кристаллических решёток: а) объёмноцентрированная; б) гранецентрированная; в) гексагональная плотноупакованная
Углерод (С) — матово-чёрный (графит) либо прозрачный (алмаз) неметалл, при температуре свыше 1827 °C алмаз переходит в графит. Плотность графита 2,23 т/м3 (алмаза — 3,51 т/м3), температура плавления — 3547 °C. Обладает хорошей электропроводностью, а также, в отличие от алмаза, низкой твёрдостью. Графит имеет слоистую структуру, слои которой могут по-разному располагаться друг относительно друга. При трении расслаивается на отдельные чешуйки.
Цементит (Fe3C) – метастабильная фаза внедрения, карбид железа, содержащий 6,67% углерода. Магнитные свойства теряет при температуре около 217 °С. Имеет высокую твёрдость (легко царапает стекло) и низкую пластичность. В зависимости от условий кристаллизации обладает различной формой (равноосные зёрна, сетка по границам зёрен, пластины, иглы). Является фазовой и структурной составляющей железоуглеродистых сплавов, составной частью ледебурита, перлита, сорбита и троостита. В сталях выделяется при охлаждении аустенита или при нагреве мартенсита. Вторичным и третичным называют цементит, выделяющийся из твёрдого раствора аустенита и феррита соответственно, в отличие от первичного цементита, выделяющегося из жидкого расплава. Распадается с образованием свободного углерода в виде графита.
Феррит – твёрдый раствор углерода и легирующих элементов в железе. Имеет объёмноцентрированную кристаллическую решётку. Различают α-феррит (твёрдый раствор углерода в α-железе) и δ-феррит (твёрдый раствор углерода в δ-железе), который появляется при температуре выше 1401 °С (высокотемпературный феррит). Нелегированный феррит относительно мягок, пластичен, сильно ферромагнитен до 768 °С. Обладает высокой растворимостью легирующих элементов, которое в большинстве случаев приводит к его упрочнению. При небольшом переохлаждении образует равноосные зёрна; при больших переохлаждениях и наличии легирующих элементов возникает по мартенситному механизму. Укрупнение зёрен аустенита приводит к выделению феррита на их границах.
Аустенит – высокотемпературная гранецентрированная модификация железа и его сплавов. В углеродистых сталях аустенит — это твёрдый раствор внедрения, в котором атомы углерода входят внутрь ячеек γ-железа во время конечной термообработки. В легированных сталях атомы металлов замещают атомы железа в кристаллической решётке. В чистом железе существует в интервале температур 910-1401 °С. В углеродистых сталях аустенит существует при температурах не ниже 723 °С.
Перлит – структурная составляющая железоуглеродистых сплавов, представляющая собой смесь фаз феррита и цементита (в легированных сталях — карбидов). Является продуктом распада аустенита при сравнительно медленном охлаждении ниже 727 °C. При этом γ-железо переходит в α-железо, избыточный углерод выделяется в форме цементита и карбидов. В зависимости от формы различают перлит пластинчатый (основной вид перлита, обе фазы имеют форму пластинок) и зернистый (округлые зёрнышки, глобули, цементита располагаются на фоне зёрен феррита). С увеличением переохлаждения растёт число колоний перлита (участков с однообразной ориентацией пластинок феррита и цементита либо карбидов), а сами пластинки становятся более тонкими. Механические свойства перлита зависят от межпластиночного расстояния (суммарная толщина пластинок обеих фаз): чем оно меньше, тем выше значение предела прочности и предела текучести и ниже критическая температура хладоломкости. При перлитной структуре облегчается механическая обработка стали. Дисперсные и высокодисперсные разновидности перлита называют сорбитом и трооститом соответственно.
Ледебурит – структурная составляющая железоуглеродистых сплавов (главным образом, чугунов), представляющая собой смесь аустенита и цементита в интервале температур 723-1147 °C или феррита и цементита ниже 723 °C. Основная фаза, инициирующая зарождение ледебурита, — цементит. На пластинке цементита, зародившейся в жидкости, разрастается плоский дендрит аустенита. Далее идёт сравнительно быстрый парный рост взаимно проросших кристаллов обеих фаз. Каждая из фаз в пределах одной колонии ледебурита непрерывна, то есть относится к одному кристаллу. Ледебурит обладает высокими твёрдостью и хрупкостью.
Мартенсит – микроструктура игольчатого вида, наблюдаемая в закалённых металлических сплавах и в некоторых чистых металлах, которым свойствен полиморфизм (существование кристаллических веществ с одинаковым составом, но с разной структурой). Основная структурная составляющая закалённой стали, представляющая собой упорядоченный пересыщенный твёрдый раствор углерода в α-железе такой же концентрации, как у исходного аустенита.
Бейнит – игольчатый троостит, структура стали, образующаяся в результате промежуточного превращения аустенита. Состоит из смеси частиц пересыщенного углеродом феррита и карбида железа.
Список литературы
- Сажин В.Б. Иллюстрации к началам курса «Основы материаловедения». — М.: ТЕИС, 2005. — 156 с.
- Свирская С.Н., Трубников И.Л., Летовальцев А.О. Методическое пособие к теме «Диаграмма состояния железо-углерод». — Ростов-на-Дону: Ростовский государственный университет, 2006. — 16 с.
| < Введение в материаловедение | Содержание | Чугуны > |

Пока нет комментариев